PARTAGEZ AVEC DES AMIS:
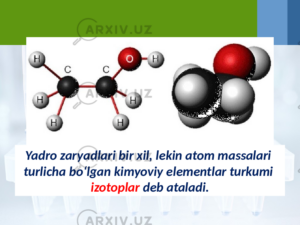
La composition du noyau atomique. Isotopes
Le nombre de masse d'un élément est égal à la somme du nombre de protons et du nombre de neutrons dans le noyau atomique :
où - le nombre de protons, - le nombre de neutrons.
Un type d'atomes du même élément avec le même numéro atomique mais des masses différentes isotopes est appelé Par exemple, les isotopes du potassium
l'isotope a 19 protons, 39 — 19 = 20 neutrons
l'isotope a 19 protons, 40 — 19 = 21 neutrons
l'isotope a 19 protons, 41 — 19 = 22 neutrons
Exemple 1. Il est constitué d'un mélange de bore et d'isotopes. La masse atomique moyenne du bore est de 10,82. Quel pourcentage d'atomes de chaque isotope contient le bore ?
Solution : Nous prenons la masse totale des isotopes du bore comme 100 %. Si la composition en pourcentage de l'isotope est égale à x, elle sera égale à 100-x. A partir de là, une équation algébrique exprimant le bilan de masse de l'atome B en pourcentage est créée :
C'est
10x+1100-11x =1082 de cela
x = 18 .
Ainsi, q18% est égal à 100-18q82%.
Exemple 2. Le chlore naturel est composé d'un mélange de 75,4 % et 24,6 % d'isotopes. Calculer la masse atomique relative moyenne du chlore.
Solution : Ce problème est l'inverse de l'exemple 1. Par conséquent, définissons la masse moyenne de chlore par x et créons une équation algébrique comme suit :
35.75,4 + 37.24,6 q 100x ðde ce
xq 35,46 amb
Ainsi, la masse atomique relative moyenne du chlore est de 35,46 amb.
Problèmes pour une solution indépendante
-
Déterminez combien de protons et combien de neutrons se trouvent dans les noyaux des atomes suivants : 1531P; 1941K; 1225mg; 2040Californie; 3065Zn; 3581Br; 46104Pd ; 50122Sn; 56130Ba ; 78188Pt.
-
Dans le brome, qui a une masse atomique relative de 79,916 3579Marque 3581Trouver le pourcentage de Br isop.
-
Lithium 36Lee et 37Il est constitué d'un mélange de Li et sa masse atomique relative moyenne est de 6,94. Trouver le pourcentage d'isotopes de lithium.
-
argent 47107Ag et 47109Il est constitué d'un mélange d'Ag et sa masse atomique relative moyenne est de 107,88. Trouvez le pourcentage d'isotopes d'argent.
-
Néon naturel 90% 1020Ne et 10% 1022Ne est composé d'un mélange d'isotopes. Calculer la masse atomique relative moyenne du néon.
-
Cuivre Naturel 27% 2965Cu et 73% 2963 Cu est composé d'un mélange d'isotopes. Calculer la masse atomique relative moyenne du cuivre.
-
Magnésium 78,6% 1224Mg et 11,29% 1225Mg est composé d'un mélange d'isotopes. Calculer la masse atomique relative moyenne du magnésium.
-
Bor 510Bande 511Il est constitué du composé B et sa masse atomique relative moyenne est de 10,81. H3BO3 teneur en acide 511Combien y a-t-il de B ?